Un uomo di 76 anni, iperteso, diabetico non insulino-dipendente, con familiarità per patologie cardiovascolari, giungeva in Pronto Soccorso per dispnea persistente associata ad agitazione psicomotoria, peggiorata negli ultimi due giorni.
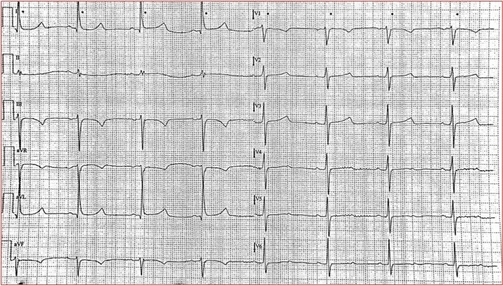
Durante l’osservazione in PS andava incontro ad episodio sincopale. L’ECG mostrava un blocco atrioventricolare di terzo grado con contestuale sovraslivellamento del tratto ST nelle derivazioni inferiori e nelle laterali e sottoslivellamento speculare nelle derivazioni D1-AVL e V1-V-3 (figura 1). L’ecocardiogramma documentava una marcata riduzione della funzione contrattile del ventricolo sinistro con acinesia delle pareti inferiore ed inferolaterale, ipocinesia della parete anteriore (FE 35%). Gli esami ematochimici mostravano un iniziale rialzo degli enzimi di miocardionecrosi (Ck-Mb 20 U/l; Troponina HS 61 ng/l ed elevati valori di creatininemia (2.3 mg/dL).

Dopo essere stato pretrattato con 4000 UI di eparina e con 250 mg di acido acetilsalicilico ev in bolo, il paziente è stato condotto d’urgenza in sala di emodinamica, ma durante la monitorizzazione elettrocardiografica pre-procedurale si assisteva ad una completa regressione delle anomalie elettrocardiografiche, con ritorno del tratto ST all’isoelettrica, scomparsa del blocco atrioventricolare e progressiva stabilizzazione delle condizioni emodinamiche (figura 2).
L’esame angiografico mostrava una stenosi intermedia alla fine del primo tratto della coronaria destra con evidenza di un notevole carico trombotico poco più a valle (Thrombus grade 4), in presenza tuttavia di un flusso TIMI conservato. L’arteria discendente anteriore presentava due stenosi critiche al tratto medio, mentre il ramo circonflesso era esente da lesioni angiograficamente significative (figura 3).
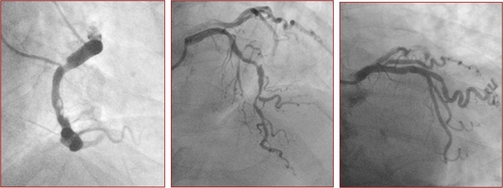
In considerazione dell’elevato burden trombotico, del conservato flusso TIMI e dell’importante rialzo della creatininemia, si è deciso di iniziare una duplice terapia antiaggregante (ASA e ticagrelor) più terapia anticoagulante infusionale (25000 UI UFH/24h) e differire la procedura di angioplastica.
Due giorni dopo il paziente è stato riportato in sala di emodinamica con evidenza di parziale risoluzione della trombosi intracoronarica. Uno studio tomografico intravascolare con OCT ha permesso di riclassificare la stenosi a monte come una vecchia ulcerazione di placca senza segni di instabilità, con una area minima luminale di 11 mm2, pertanto è stato deciso di non eseguire stenting della suddetta lesione (figura 4).

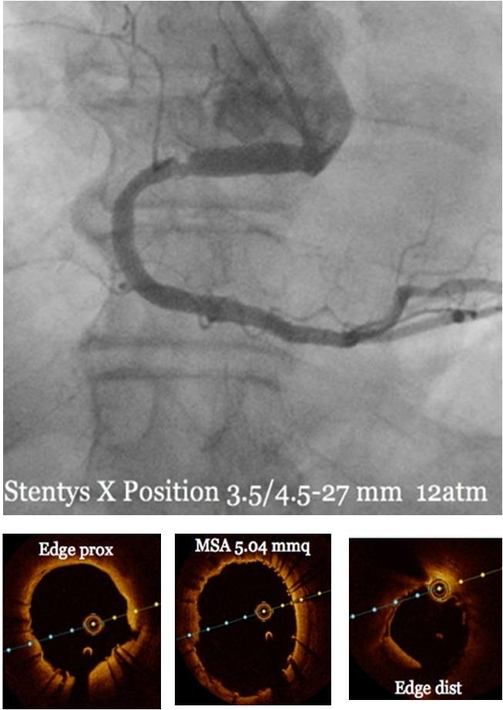
Al contrario, l’ulcerazione di placca responsabile della trombosi intracoronarica con ancora una lieve residua apposizione trombotica è stata efficacemente trattata con impianto di stent autoespandibile Stentys X position S 3.5-4.5 x 27 mm (stenting diretto). Un pullback OCT finale mostrava una buona apposizione delle maglie dello stent, assenza sia di dissezioni agli edges che di protusione di materiale trombotico tra le maglie dello stent (figura 5).
Durante lo stesso ricovero il paziente è stato sottoposto a completamento della procedura di rivascolarizzazione su IVA. L’ecocardiogramma alla dimissione mostrava un miglioramento della cinetica regionale con parziale recupero della funzione contrattile (FE 45%).
Al follow-up ecocardiografico annuale la funzione sistolica è ulteriormente aumentata ed il paziente mostra un buon compenso emodinamico, in assenza di segni clinici e strumentali di scompenso cardiaco.
DISCUSSIONE
Come dimostrato da Lemkes JS e coll. tra i pazienti con STEMI transitorio, la terapia invasiva immediata non è superiore a quella attendistica nel ridurre l’estensione dell’infarto (figura 6) [1].

In presenza di un elevato carico trombotico con flusso periferico conservato seguire il “riflesso oculostenotico”, non tenendo in considerazione dell’importanza dell’impairment del microcircolo in caso di embolizzazione periferica, potrebbe portare ad una inefficace riperfusione, malgrado una buona ricanalizzazione. Sapere quando non fare spesso è la cosa più difficile!
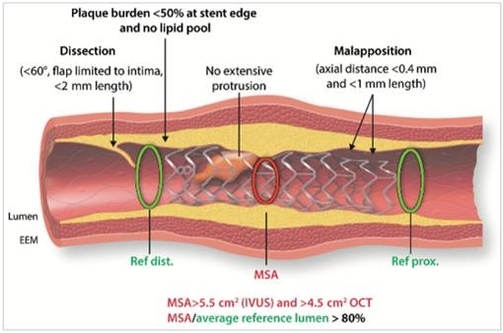
L’utilizzo della metodica OCT ha permesso sia di cambiare la strategia di stenting limitando il trattamento solo alla lesione colpevole, sia di verificare un ottimo risultato dell’angioplastica. Come suggerito da Raber e coll. i criteri OCT che definiscono ottimale un impianto di stent coronarico sono i seguenti (figura 7) [2]:
- assenza di malapposizione (limite di tolleranza: distanza lume-stent <0.4 mm per meno di 1 mm di lunghezza)
- assenza dissezione (limite di tolleranza: flap limitato all’intima per una lunghezza <2 mm con un’estensione circonferenziale <60°)
- assenza di protusione di materiale trombotico intraluminale
- burden di placca <50% agli edges
- area minima intrastent > 4.5 mmq.
La scelta di utilizzare stent autoespandibili è stata guidata dal grosso calibro del vaso e dalla necessità di ottenere una progressiva dilatazione dello stent nel tempo, soprattutto dopo un completo riassorbimento del trombo intraluminale. Inoltre il disegno a maglie strette di questa tipologia di stent avrebbe incarcerato il trombo residuo impedendone l’embolizzazione distale e la protusione intrastent. Oggigiorno questi stent non sono più disponibili nei nostri laboratori di emodinamica per riscontro di problemi di geographical missing con il delivery system. Tuttavia il forte razionale che questa tipologia di stent trova in situazioni simili a quella descritta sta spingendo la comunità scientifica a reintrodurli in commercio con qualche miglioria.
BIBLIOGRAFIA
- Lemkes JS, Janssens GN, van der Hoeven NW, van de Ven PM, Marques KMJ, Nap A, van Leeuwen MAH, Appelman YEA, Knaapen P, Verouden NJW, Allaart CP, Brinckman SL, Saraber CE, Plomp KJ, Timmer JR, Kedhi E, Hermanides RS, Meuwissen M, Schaap J, van der Weerdt AP, van Rossum AC, Nijveldt R, van Royen N. Timing of revascularization in patients with transient ST-segment elevation myocardial infarction: a randomized clinical trial. Eur Heart J. 2019;40:283-291
- Räber L, Mintz GS, Koskinas KC, Johnson TW, Holm NR, Onuma Y, Radu MD, Joner M, Yu B, Jia H, Meneveau N, de la Torre Hernandez JM, Escaned J, Hill J, Prati F, Colombo A, Di Mario C, Regar E, Capodanno D, Wijns W, Byrne RA, Guagliumi G.Clinical use of intracoronary imaging. Part 1: guidance and optimization of coronary interventions. An expert consensus document of the European Association of Percutaneous Cardiovascular Interventions. 2018;14:656-677