Un ragazzo di 23 anni, con storia clinica muta e privo di familiarità per CVD e SCD, presenta due episodi di perdita di coscienza transitoria, rispettivamente nel 2017 e nel 2019, avvenuti in circostanze e modalità analoghe, durante la guida di automobile nelle ore notturne, in assenza di prodromi, con rapida e spontanea ripresa dello stato di coscienza.
Dagli elementi anamnestici non ci sono elementi che permettono di escludere con certezza alcuna delle possibili eziologie di tali episodi di perdita di coscienza1 (figura 1).
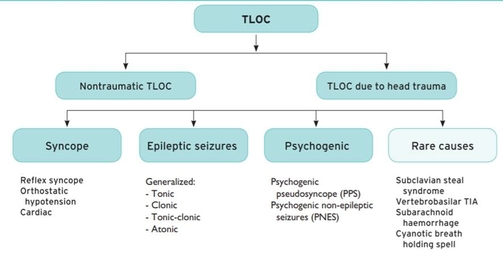
Successivamente al secondo episodio, il paziente, anche in considerazione di una familiarità di primo grado per epilessia indotta da stimoli luminosi, eseguiva una visita neurologica ed una RMN cerebrale e dei vasi epiaortici con mdc, da cui non emergevano elementi patologici di rilievo.
Giungeva quindi al nostro Centro per indagare una possibile genesi cardiogena di tali episodi. Il paziente si presentava in sostanziale benessere clinico, asintomatico dal punto di vista cardiovascolare, in classe funzionale NYHA I.
Dalla revisione della documentazione in visione ed in particolare della documentazione dell’accesso in PS di un Presidio Ospedaliero del territorio in merito al secondo episodio di perdita di coscienza, non si rilevavano elementi patologici, in particolare gli esami ematochimici di routine risultavano nella norma, lo screening tossicologico risultava negativo e non venivano segnalati eventi aritmici al monitoraggio elettrocardiografico.
Alla nostra valutazione i parametri vitali e l’obiettività risultavano nella norma (PA 120/80 mmHg, SpO2 96% in AA), in assenza di segni di scompenso cardio-circolatorio.
All’ECG (figura 2) si evidenziava un ritmo sinusale alla FC di 76 bpm, un intervallo PR corto (110 ms) in assenza di segni di pre-eccitazione ventricolare, ed un ritardo aspecifico di conduzione intraventricolare (QRS 105 ms) con piccole onde q in sede inferiore ai limiti della significatività.
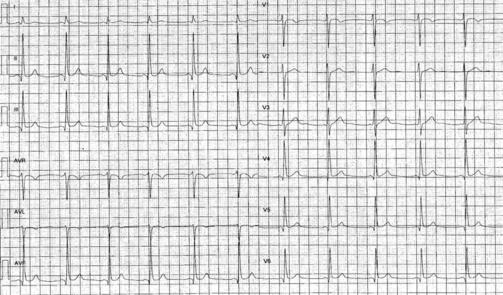
In considerazione di tali elementi ECGgrafici ai limiti ma comunque non francamente patologici, veniva richiesto un ecocardiogramma transtoracico (figura 3), dove veniva evidenziata, nel contesto di normali volumi e funzione sistolica biventricolari in assenza di valvulopatie, una formazione simil-aneurismatica in sede antero ed inferolaterale apicale, con parete assottigliata e contrattile ed ipertrabecolatura, dotata di ampia comunicazione con il ventricolo sinistro, in assenza di segni di trombosi endocavitaria.
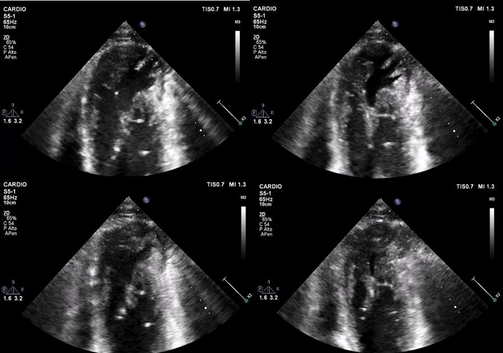
Al fine di caratterizzare meglio la formazione sopra descritta, veniva eseguita una RMN cardiaca senza e con mdc (figura 4):
- si confermava la presenza della formazione contrattile simil-aneurismatica apicale e i normali volumi e funzione sistolica globale e segmentaria biventricolare;
- dallo studio delle sequenze T1 e T2 mapping, perfusione di primo passaggio e late gadolinium enhancement (LGE), la parete della formazione, così come tutto il restante miocardio, risultava costituita dalle normali componenti endo, mio ed epicardiche, con normali tempi di rilassamento T1 e T2, in assenza di deficit di perfusione di primo passaggio e di LGE nelle sequenze tardive;
- si confermava l’assenza di altre anomalie strutturali cardiache.

Nell’ambito delle formazioni simil aneurismatiche del ventricolo sinistro, le entità cliniche più comuni sono costituite dall’aneurisma, dallo pseudoaneurisma e dal diverticolo del ventricolo sinistro. Ciascuna di queste entità, sebbene presenti alcune analogie, risulta comunque non compatibile con la formazione descritta nel nostro paziente. In particolare:
- l’aneurisma ventricolare sinistro, congenito o acquisito, risulta caratterizzato da una parete assottigliata, ma quest’ultima è costituita da tessuto fibrotico (scar) non contrattile/discinetico, con alterazioni tipiche del segnale alla RMN cardiaca (LGE)
- lo pseudoaneurisma ventricolare si presenta come soluzione di continuo della parete ventricolare contenuta dal pericardio da un trombo organizzato o da un ematoma.
- il diverticolo ventricolare sinistro si presenta con una parete costituita dalle normali strutture cardiache, contrattile, ma la cavità diverticolare presenta un colletto di comunicazione ristretto con la cavità ventricolare sinistra. Inoltre questa entità clinica tende ad associarsi ad altre anomalie cardiache o extracardiache congenite della linea mediana.
Abbiamo pertanto formulato la diagnosi di Doppia camera ventricolare sinistra (Double chambered left ventricle, DCLV), una rara anomalia cardiaca congenita caratterizzata dalla suddivisione del ventricolo sinistro in due camere ventricolari mediante l’interposizione di trabecole di miocardio. La cavità ventricolare accessoria presenta una parete che è costituita dalle normali strutture endo, mio ed epicardiche, con vitalità e cinetica conservata.
In letteratura sono descritti circa 29 casi in tutto il mondo, ma la reale incidenza di tale condizione potrebbe essere sottostimata, dal momento che nella maggior parte dei casi, come nel nostro, la diagnosi risulta essere incidentale.
Non è chiaro il meccanismo fisiopatologico alla base di tale anomalia, che potrebbe costituire una variante focale del miocardio non compatto2-3 . Il DCLV può presentarsi come anomalia isolata o associato ad altre anomalie congenite. La maggior parte dei casi risulta asintomatica, e l’anomalia costituisce un riscontro accidentale4. L’ECG può presentare reperti aspecifici, come blocco di branca sinistra, emiblocco anteriore sinistro o ritardi aspecifici di conduzione intraventricolare3-4. L’ecocardiogramma è l’esame diagnostico di primo livello che permette di evidenziare l’aspetto simil-aneurismatico della camera ventricolare accessoria. La RMN cardiaca costituisce l’esame diagnostico dirimente che permette la diagnosi differenziale con le altre formazioni simil-aneurismatiche del ventricolo sinistro, come già esposto sopra5-9. La ventricolografia e la TC con mdc possono costituire alternative alla RMN se quest’ultima non risulta possibile/disponibile10.
Anche alla luce della limitata casistica in letteratura, da cui peraltro non si evince un significativo aumento del rischio aritmico nei pazienti affetti da DCLV, con un solo caso di DCLV associata a TV sostenuta monomorfa in assenza di una chiara relazione causa-effetto11 e persistendo l’incognita diagnostica in merito al quesito clinico iniziale, a completamento diagnostico venivano eseguiti:
- Coronarografia (figura 5): coronarie indenni da lesioni angiograficamente significative. Normale origine e decorso.

- Studio elettrofisiologico endocavitario: nella norma gli intervalli AH e HV ed il SNRT. Assente fisiologia da doppia via nodale. Punto di Wenckebach anterogrado 270 ms, retrogrado 450 ms. Non inducibilità di aritmie ventricolari con doppio sito di stimolazione fino a 3 extrastimoli.
- Loop recorder esterno (tuttora in corso): non eventi aritmici patologici.
Terapia e follow up: la gestione terapeutica dei pazienti con doppia camera ventricolare sinistra risulta essere individualizzata. I pazienti asintomatici, privi di segni di scompenso cardiaco, di disfunzione ventricolare sinistra e privi di altre anomalie cardiache congenite necessitanti di correzione, vengono trattati conservativamente4.
Nel nostro paziente, in considerazione dell’assenza di segni di disfunzione ventricolare sinistra e di alcuna sintomatologia, non è stata intrapresa alcuna terapia medica.
In merito alla prognosi di tali pazienti, i dati di follow up longitudinale a medio-lungo termine risultano essere scarsi. Analogamente ad altri contesti fisiopatologici, è stato proposto l’utilizzo della metodica ecocardiografica dello speckle-tracking per la valutazione della funzione sistolica longitudinale come predittore di disfunzione sistolica sinistra12.
Abbiamo pertanto impostato un follow up cardiologico periodico comprensivo di ecocardiogramma ed RMN cardiaca, e contemporaneamente riferito il paziente ad un Centro Neurologico di III livello per la prosecuzione dell’iter diagnostico neurologico.
Bibliografia:
- 2018 ESC Guidelines for the diagnosis and management of syncope, European Heart Journal, 2018; 398:1883–1948
- Novo G, Dendramis G, Marrone G, Novo S, Thiene G. Left ventricular noncompaction presenting like a double-chambered left ventricle. J Cardiovasc Med (Hagerstown) 2015;16: 522-4.
- Gufler H, Anderson RH, Annette M, Voigtlaender T. Doublechambered left ventricle in a patient with chest pain. Clin Res Cardiol 2018;107:1180-2
- Yuan SM. Double-chambered Left Ventricle: Clinical Features Comparison between Children and Adults. J Coll Physicians Surg Pak. 2019;29:1087-1091.
- Nacif MS, Mello RA, Lacerda Junior OO, Sibley CT, Machado RA, Marchiori E. Double-chambered left ventricle in an adult: diagnosis by CMRI. Clinics (Sao Paulo). 2010;65:1393-1395.
- Masci PG, Pucci A, Fontanive P, et al. Double-chambered left ventricle in an asymptomatic adult patient. Eur Heart J Cardiovasc Imaging. 2012;3:E1–E3.
- Mordi I, Carrick D, Tzemos N. Diagnosis of double-chambered left ventricle using advanced cardiovascular imaging. Echocardiography. 2013;7:E206–E208.
- Ole A. Breithardt, Dieter Ropers, Theresa Seeliger, Axel Schmid, Johannes von Erffa, Christoph Garlichs, Werner G. Daniel, Stephan Achenbach, A heart within the heart: double-chambered left ventricle, European Journal of Echocardiography, 2008; 9: 739-41
- Zhang X, Wang J, Cao Y, Zheng L, Li P, Duan X, Wang F. Diagnosis of double-chambered left ventricle using echocardiography. Echocardiography. 2020;37:1095-1100.
- Sanz J, Rius T, Kuschnir P, Macaluso F, Fuster V, Poon M. Double-chambered left ventricle: Complete characterization by cardiac magnetic resonance and multidetector-row computed tomography. Circulation 2004; 110:e502-3.
- Sharma S, Dinwoodey DI, Chaudhry GM, Labib SB. Congenital Double-Chambered Left Ventricle Presenting as Monomorphic Ventricular Tachycardia. CASE (Phila). 2019;3:51-55.
- Harada K, Mori K, Ichimiya C, Terada N, Iima T, Harada T, Fujisawa K, Kawata A, Okada A, Yamamoto H, Fujinaga H. Five-year follow-up two-dimensional speckle tracking echocardiography in a juvenile with a double-chambered left ventricle. Echocardiography. 2017;34:791-793