Un uomo di 25 anni veniva ricoverato per dispnea da sforzi lievi ed edemi declivi, negli ultimi 15 giorni erano stati riscontrati un aumento ponderale di circa 20 kg ed un forte incremento della circonferenza addominale.
L’esame obiettivo metteva in evidenza una PA 130/70 mmHg, una FC 85/min ed una FR 25/m; era presente un decubito semi-ortopnoico obbligato, con addome globoso per la presenza di ascite ed edemi declivi bilaterali estesi fino alla radice della coscia. Il paziente inoltre presentava un habitus marfanoide.
La sua anamnesi cardiologica infatti documentava all’età di 16 anni una dissezione aortica acuta di tipo A con insufficienza aortica severa sottoposta ad intervento di Bentall-De Bono, complicato da infarto miocardico intraoperatorio in sede inferiore, trattato con by-pass aorto-coronarico per l’arteria coronaria destra. Veniva contestualmente diagnosticata la Sindrome di Marfan con familiarità per i genitori e i tre figli.
All’età di 20 anni era stato inoltre sottoposto a sostituzione aortica protesica per aneurisma dissecante cronico dell’arco aortico e dell’aorta toracica (figura 1), complicata da ematoma peri-aortico ed ischemia midollare con residua ipostenia dell’emisoma. Insorgeva contestualmente una fibrillazione atriale.
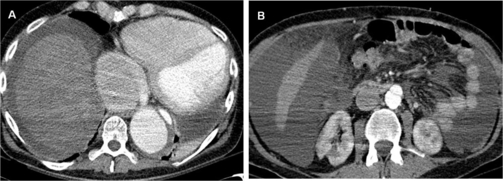
All’età di 21 anni effettuava un ricovero per scompenso cardiaco durante il quale veniva riscontrata una severa disfunzione ventricolare sinistra (FE 20%) e pertanto si ottimizzava la terapia cardiologica e successivamente veniva impiantato il defibrillatore cardiaco (ICD).
Nei 3 anni seguenti si sono verificati ricorrenti episodi di scompenso cardiaco, trattati efficacemente con diuretici endovena. All’età di 24 anni ulteriore episodio di scompenso cardiaco per il quale effettuava ricovero ospedaliero con evidenza di insufficienza mitralica severa da rottura di corda tendinea e flail del lembo anteriore (figura 2), insufficienza tricuspidalica severa ed ipertensione polmonare. Veniva pertanto effettuato intervento di sostituzione valvolare mitralica con protesi meccanica ed anuloplastica tricuspidalica.

La sua storia clinica si caratterizzava inoltre per ipertiroidismo, pregressa abitudine tabagica, storia di potus in paziente con condizioni socio-economiche non ottimali.
La terapia domiciliare comprendeva carvedilolo 6,25 mg/die, digossina 0,25 mg/die; Sacubitril/Valsartan 49/51 mg bid; Amlodipina 5 mg/die; Daxozosina 4 mg/die; Furosemide 500 mg/die; Spironolattone 50 mg/die; Warfarin secondo INR (target 2,5-3,5); atorvastatina 20 mg/die
La RX torace all’ingresso in reparto documentava la presenza di cardiomegalia con marcata congestione ilare e versamento pleurico bilaterale (figura 3).

L’Elettrocardiogramma invece documentava la presenza di fibrillazione atriale interrotta da extrasistolia ventricolare isolata e la presenza di anomalie della ripolarizzazione ventricolare in sede inferiore (figura 4).

Gli esami ematochimici all’ingresso mostravano un’alterazione degli indici di colestasi ed un marcato incremento dell’ NTproBNP (21789 pg/mL), non sostanziali alterazioni dell’emocromo e della funzionalità renale.
All’ecocardiogramma (figura 5) si documentavano: protesi valvolare aortica meccanica in sede, gradienti transprotesici nei limiti per sizing; protesi mitralica in sede con verosimile leak paravalvolare (gradiente medio 8.7 mmHg); grave dilatazione del ventricolo sinistro, con spessori parietali lievemente aumentati con ipocinesia globale ed acinesia del SIV medio-apicale e funzione globale gravemente depressa (FE 19%).

Il paziente è stato quindi sottoposto a terapia diuretica ev e dobutamina ev, con miglioramento del quadro di compenso emodinamico e della sintomatologia. In III giornata di ricovero per fugaci episodi di obnubilamento del sensorio e rilievo al monitoraggio telemetrico di run di tachicardia ventricolare, veniva interrogato l’ICD che documentava la presenza di alcuni episodi di Tachicardia Ventricolare Sostenuta trattata dal dispositivo con DC shock dopo alcuni tentativi inefficaci di ATP (figura 6):

Dopo circa 50 minuti si verificava invece un episodio di fibrillazione ventricolare sempre opportunamente riconosciuta dall’ICD e trattata con DC shock (figura 7).

Due ore dopo l’instabilità elettrica si ripresentava con un un nuovo episodio di tachicardia ventricolare sostenuta interrotta al secondo tentativo di ATP (figura 8).

In presenza di storm aritmico in paziente portatore di ICD, veniva impostata terapia con Amiodarone ev, e successivamente veniva aumentata la terapia con Carvedilolo bid per os. Il paziente veniva dimesso in terapia medica con betabloccante titolato al massimo dosaggio.
Discussione
La Sindrome di Marfan è un disturbo genetico autosomico dominante caratterizzato da circa 400 mutazioni del gene per la fibrillina-1, con una prevalenza nella popolazione generale di 1.7-1.2 per 100.000 abitanti [1,2]. La diagnosi viene fatta mediante parametri nosologici Ghent-2 che si basano sulla presenza di storia familiare insieme ad altri specifici criteri diagnostici [1,3]. Il coinvolgimento variabile di un solo organo o multi-organo (visivo, scheletrico, sistema cardiovascolare) e l’assenza di terapia, sono responsabili di un decorso della malattia cronico, severo, e a rischio di sopravvivenza [1]. Tuttavia un miglioramento in termini di terapia medica o chirurgica, può aumentare l’aspettativa di vita da 32 a 52 anni [4]. I pazienti con sindrome di Marfan presentano una cardiomiopatia primitiva caratterizzata da deficit della fibrillina-1 muscolare cardiaca che comporta disfunzione ventricolare sinistra dovuta ad ipertrofia e dilatazione, anomalie delle corde tendinee con prolasso e rigurgito valvolare ed aumentata prevalenza di sindrome di Wolff-Parkinson-White ed inoltre si può notare un interessamento cardiaco secondario a complicanze ischemiche derivate dagli interventi cardiochirurgici nell’8.7% dei casi [4]. La causa più comune di morte nei soggetti non trattati è la dissezione e la rottura dell’aorta ascendente, ma ci sono evidenze che questi pazienti siano a rischio di aritmie ventricolari e morte cardiaca improvvisa [5,6]. La dilazione ventricolare è stata associata a morte per cause aritmiche negli adulti con scompenso cardiaco, infatti anche in assenza di insufficienze valvolari, la dilatazione avviene comunemente nei Marfan ed è associata ad alterazione della ripolarizzazione che comporta in ultima analisi ad aritmie ventricolari [7]. I pazienti con Marfan hanno aumentata rigidità della parete aortica che comporta essa stessa aumentato post-carico ventricolare e quindi in ultima analisi a dilatazione.
Conclusione
La malattia di Marfan è una sindrome eterogenea caratterizzata da ampio spettro di manifestazioni cliniche. Temibile è la morte improvvisa per patologia strutturale come nell’ambito della dissezione aortica o dal punto di vista aritmologico, e quindi da dilatazione del miocardio o secondaria a complicanze ischemiche. Nel caso del paziente in esame, con scompenso cardiaco avanzato, sarebbe stato auspicabile la valutazione presso un centro trapianti specifico per la patologia. Purtroppo le condizioni socio-economiche e la storia di potus, hanno reso il nostro paziente, non candidabile. Pertanto, è stato dimesso a domicilio e gestito ambulatorialmente con terapia medica massimale e stretto monitoraggio clinico. Verrà valutata, se confermata persistenza degli eventi aritmici al monitoraggio del dispositivo ICD, la possibilità di ablazione del substrato aritmico.
Bibliografia
- Von Kodolitsch Y, De Backer J, Schüler H, et al. Perspectives on the revised Ghent criteria for the diagnosis of Marfan syndrome. Appl Clin Genet 2015;8:137–55.
- Seo GH, Kim YM, Kang E, et al. The phenotypic heterogeneity of patients with Marfan-related disorders and their variant spectrums. Medicine(Baltimore) 2018;97:e10767.
- Loeys BL, Dietz HC, Braverman AC, et al. The revised Ghent nosology for the Marfan syndrome. J Med Genet 2010;47:476–85.
- Hetzer R, Siegel G, Delmo Walter EM. Cardiomyopathy in Marfan syndrome. Eur J Cardiothorac Surg 2016;49:561–7. discussion 567-568.
- Chen S, Fagan LF, Nouri S, Donahoe JL (1985) Ventricular dysrhythmias in children with Marfan’s syndrome. Am J Dis Child 139: 273–276.
- Hoffmann BA, Rybczynski M, Rostock T, Servatius H, Drewitz I, et al. (2012) Prospective risk stratification of sudden cardiac death in Marfan’s syndrome. Int J Cardiol.
- Anji Yetman, Bornemeier R et al., Long-Term Outcome in Patients with Marfan Syndrome: Is Aortic Dissection the Only Cause of Sudden Death?. Eu Heart J 1994